
Las Reacciones Químicas
y sus Ecuaciones

¡COMENcEMOS!

¿Cuánto sabes de química?

La reacción química es un cambio en la composición de las sustancias para formar otras diferentes.
UN DATO interesante

Reacción Química

Ecuación Química
A las sustancias que inician la reacción química las denominamos reactivos y las sustancias
finales que se obtienen son los productos.


Para que los reactivos se transformen, deben romperse los enlaces que unen sus átomos.
Después, estos átomos se reagrupan de modo distinto para formar nuevos enlaces y dar
lugar a los productos.
Aprendamos a leer una ecuación química.
Haz click aquí


o escanea el código

-
Una reacción química consta de dos miembros, separados por una flecha (→) que indica el sentido de la transformación.
-
En el primer miembro escribimos las fórmulas químicas de los reactivos y, en el segundo miembro, las fórmulas químicas de los productos.
-
Si hay varios reactivos o varios productos, separamos unos y otros por medio del signo más (+).

Aquí tienes un tutorial para comprender el proceso teórico de las reacciones químicas.


tipos de reacciones químicas

La fórmula general para representar la síntesis de un compuesto químico es la siguiente


En este enlace puedes observar la parte práctica de una reacción de síntesis.
Un pequeño experimento.


Descomposición de una molécula de agua



El agua (H2O líquido) al calentarse se descompone en sus dos sustancias principales que son el Hidrógeno y el Oxígeno gaseosos.
En conclusión, una sustancia se descompone en otras más sencillas.
Aprendamos juntos
Si la fórmula del agua es H2O, ¿Cuál crees que sea el elemento que más se necesita para su síntesis?





Arriba podemos ver la fórmula general para representar una reacción de doble desplazamiento.
A continuación podemos observar un ejemplo:

Imagínalo como un "intercambio de parejas" en un baile: si tienes los reactivos AX y BY, el catión A se une al anión Y, mientras que el catión B se une al anión X, resultando en AY y BX. Para que esta reacción ocurra de forma perceptible, generalmente uno de los productos formados debe ser un sedimento sólido (precipitado), un gas o agua, lo que "fuerza" a los iones a dejar de estar libres en la solución.



Existen otros tipos de reacciones que detallamos a continuación:

La combustión es una reacción química de oxidación rápida que desprende una gran cantidad de energía en forma de luz y calor. Para que ocurra, es indispensable la presencia de un combustible (la sustancia que se quema) y un comburente (generalmente el oxígeno del aire). Cuando una combustión es completa, los productos resultantes son siempre dióxido de carbono (CO2) y agua (H2O), liberando la energía almacenada en los enlaces químicos del combustible.





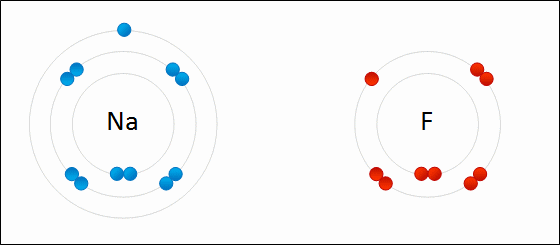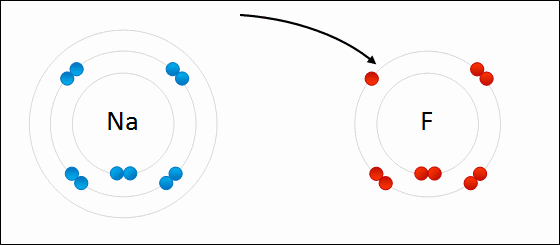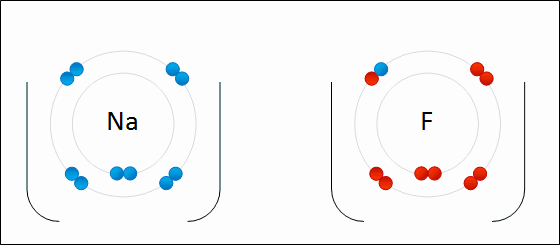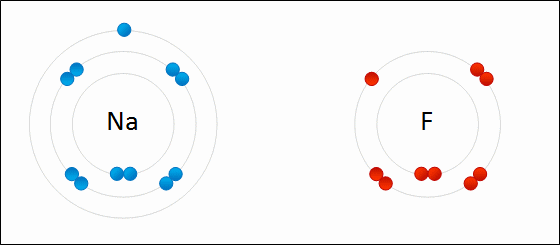
Es el intercambio de electrones entre los átomos de las sustancias reaccionantes.
Se define la oxidación como el proceso en el cual un átomo o ion pierde electrones, lo que provoca un aumento en su número de oxidación.
Por el contrario, la reducción ocurre cuando un átomo o ion gana electrones, disminuyendo su número de oxidación.
Ambos procesos son simultáneos e inseparables: si una sustancia se oxida, necesariamente otra debe reducirse, permitiendo así el flujo de energía química.

Escala de ph
Es una herramienta para medir el grado de acidez o alcalinidad de una solución, situando el valor 7 como neutro, los valores inferiores como ácidos y los superiores como básicos o alcalinos, proporcionando ejemplos de sustancias comunes para ilustrar estos niveles.



Cuando un ácido reacciona con una base se obtienen como productos una sal y agua. A este proceso se le conoce como Reacción de Neutralización.

¿Sabías Qué?
La formación de la sal común de mesa, o cloruro de sodio (NaCl), es el resultado de una reacción de neutralización donde se combinan un ácido fuerte, el ácido clorhídrico (HCl), y una base fuerte, el hidróxido de sodio (NaOH).
En este proceso, que ocurre típicamente en disolución acuosa, los iones de hidrógeno (H+) del ácido se unen con los iones hidroxilo (OH-) de la base para formar moléculas de agua (H2O), mientras que los iones de sodio (Na+) y cloro (Cl-) permanecen en la solución. Esta interacción es fundamental porque logra "neutralizar" las propiedades corrosivas de ambos reactivos, estabilizando el pH de la mezcla hacia un valor neutro de 7.
Finalmente, para obtener la sal sólida que conocemos, el agua debe evaporarse, permitiendo que los iones de sodio y cloro se atraigan electrostáticamente y se organicen en una estructura cristalina cúbica, dando lugar a los cristales de sal que utilizamos diariamente.




En conclusión, las reacciones químicas no solo implican un cambio en la estructura de una sustancia, sino también un intercambio constante de energía y electrones, lo que permite desde el funcionamiento de nuestras células hasta la creación de materiales industriales, rigiéndose siempre por la ley de conservación de la materia.




